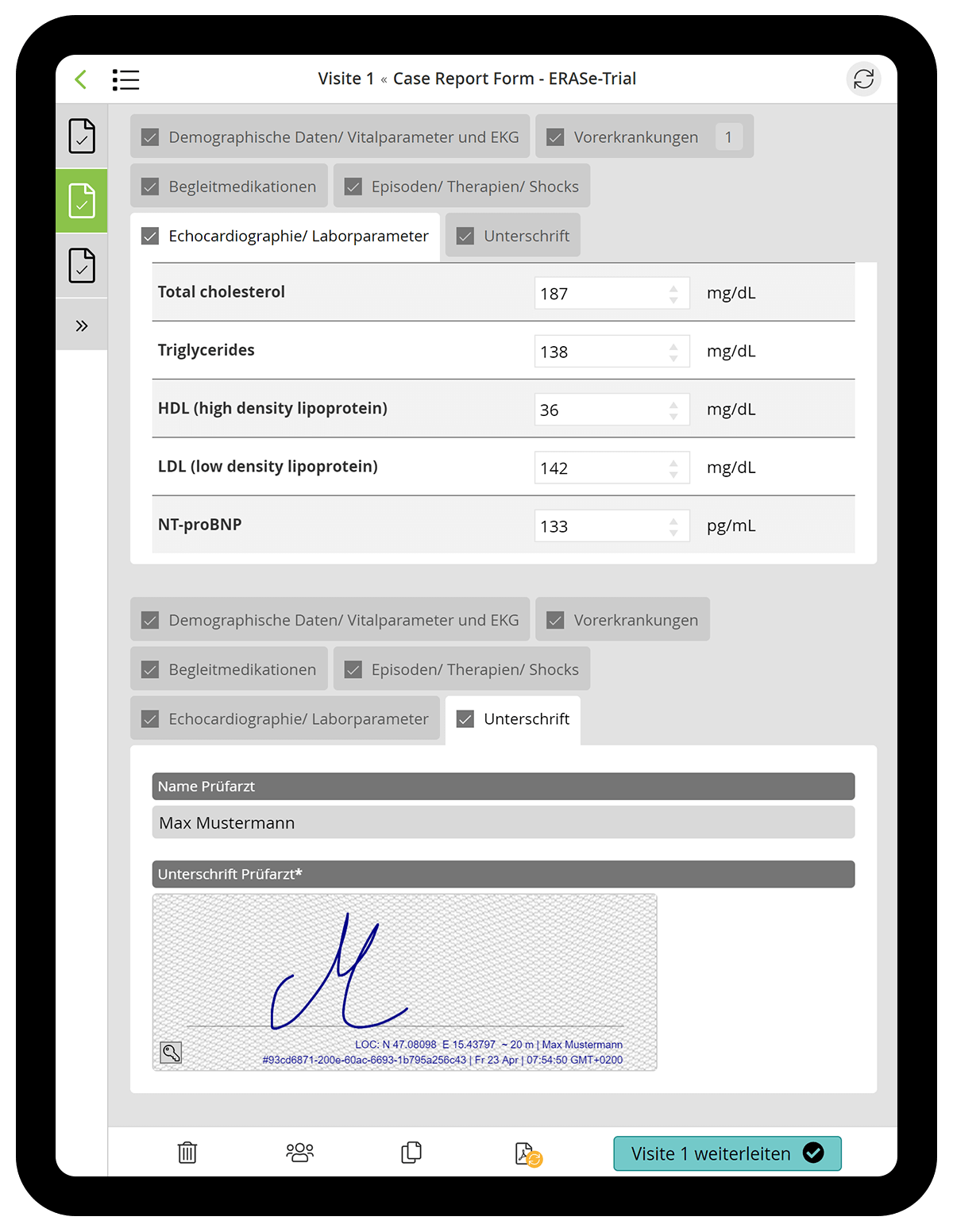
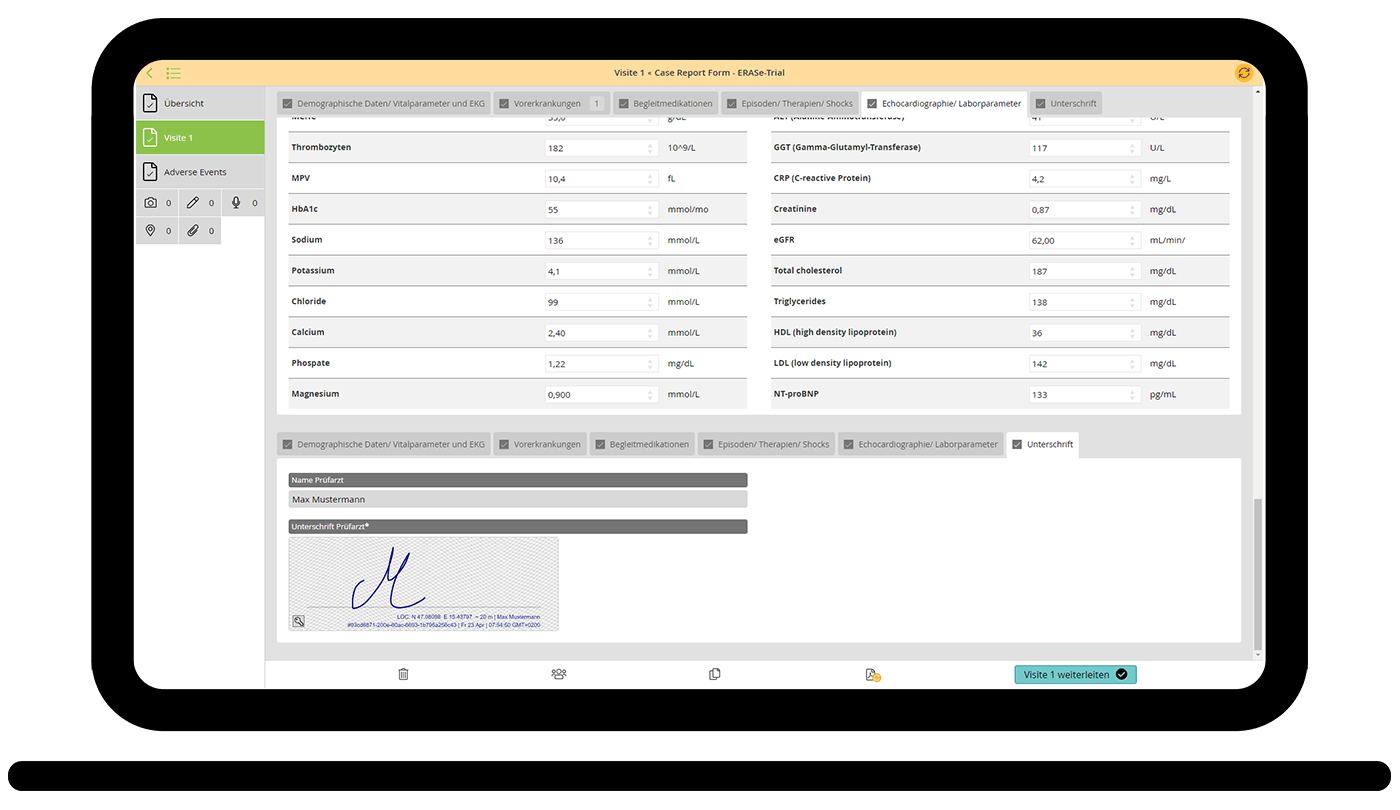
Das Projektteam der klinischen Studie erfasst alle Patientendaten durchgängig digital mit der HybridForms App: Die Protokolle der Visiten im Rahmen der Medikamentenstudie werden in den teilnehmenden Kliniken digital und standortübergreifend in einem mehrstufigen Prozess mit HybridForms dokumentiert.
HybridForms: Digitale Formulare in der medizinischen Forschung
In den Case Report Forms werden die Benutzer strukturiert durch die Anwendung geführt. Pflichtfelder sind eindeutig markiert, Eingaben werden automatisch validiert, das System zeigt Warnmeldungen bei Fehlern an. Damit ist sichergestellt, dass erfasste Daten wie Vitalparameter, Vorerkrankungen, Therapie, Medikation und Laborparameter vollständig und genau sind – ein wichtiges Kriterium für den Erfolg einer Studie.
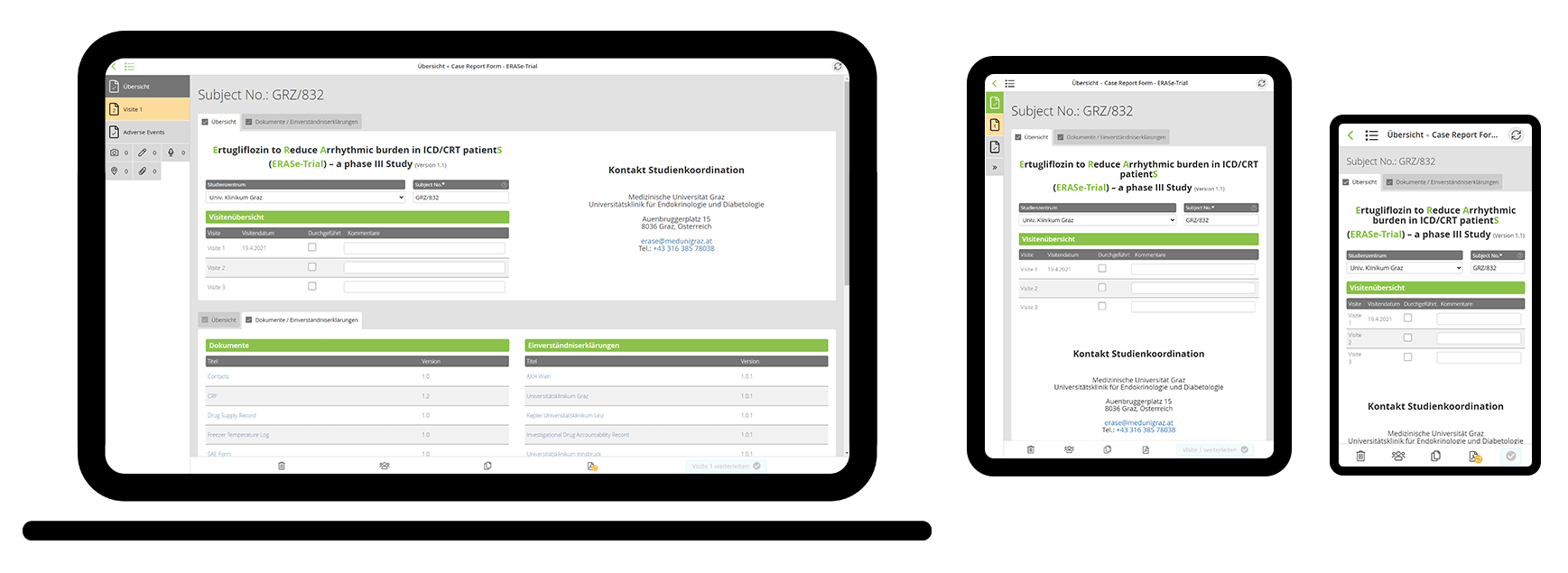
Digital erfasste Daten sind sicherer als Papier und schneller verfügbar. Alle Daten auf den Endgeräten werden verschlüsselt und automatisch mit dem Core-Server synchronisiert, die Informationen stehen damit sofort zentral zur Verfügung. Standortübergreifende Studien können damit auch in verteilten Teams zuverlässig und ohne Verzögerungen dokumentiert werden – effizient, sicher und transparent.
Die Änderungen bei jedem Formular-Update werden mit Audit Trail protokolliert – eine wichtige Funktion zur Qualitätssicherung. Durch die Rückverfolgung sind Details wie Version, Datum, Uhrzeit, Benutzer und Art der Änderung jederzeit nachvollziehbar.

»Für unser multizentrisches Studienprojekt waren wir auf der Suche nach einem elektronischem CRF-System, welches ein intuitives Arbeiten ermöglicht, einen logischen Aufbau verfolgt und für die Studienmitarbeiter:innen leicht zu bedienen ist. Zusätzlich musste das System den vorgegebenen Regularien entsprechen (Monitoring, Audit Trail, Rollenfunktionen, Datenexport). Diese Anforderungen konnten HybridForms und Kapsch BusinessCom zu unserer vollsten Zufriedenheit erfüllen.«

»Mit der HybridForms Plattform war es uns als Digitalisierungspartner möglich, die Anforderungen unserer Kunden optimal abzudecken und eine einfache, intuitive Lösung zur digitalen Datenerfassung auf mobilen Endgeräten bereitzustellen. Speziell der Einsatz der HybridForms Funktionalitäten ›Stages‹ und ›Audit Trail‹ ermöglichten die vollumfängliche Abdeckung des mehrstufigen Review-Prozesses sowie die lückenlos nachvollziehbare Abwicklung der klinischen Doppelblind-Medikamentenstudie.«
Workflow Stages mit stufenweiser Bearbeitung von Formularen durch verschiedene Benutzer mit unterschiedlichen Sichtbarkeiten
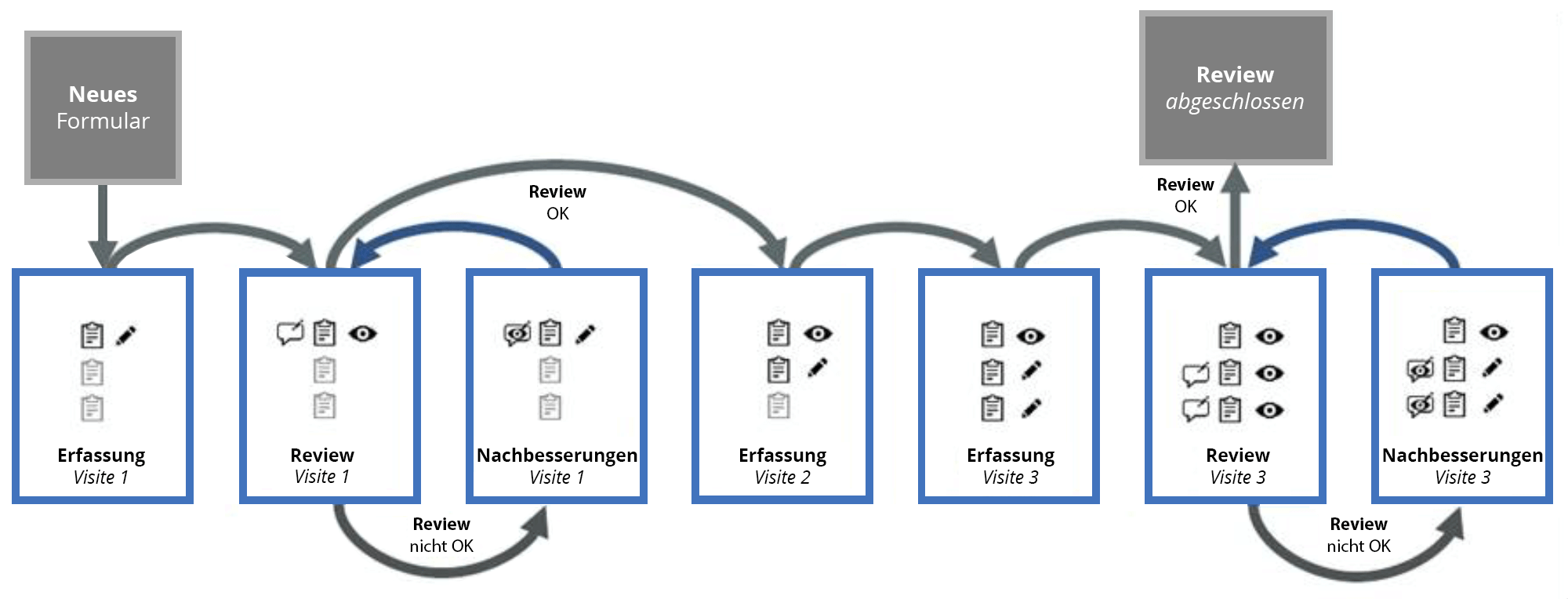
HybridForms mit sicheren Enterprise-Features und stufenweisem Formular-Workflow für die Einhaltung von Compliance-Richtlinien bei klinischen Studien
GCP – Good Clinical Practice
Gute Klinische Praxis ist ein internationaler ethischer und wissenschaftlicher Standard für die Planung, Durchführung, Dokumentation und Berichterstattung von klinischen Prüfungen am Menschen.
Zur Qualitätssicherung der Prozesse und als Standard Operating Procedure (SOP) muss die detaillierte textliche Dokumentation inklusive Änderungsmanagement und Prüfung der Daten sichergestellt werden. Die jederzeitige Rückverfolgbarkeit von Änderungen ist dabei ein zentrales Thema.